 |
 |
Kleine Moleküle: |
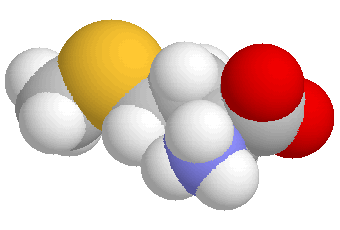
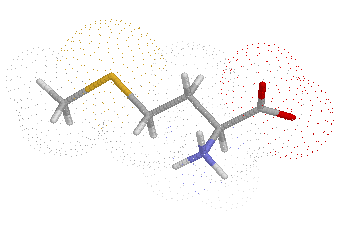
| Methionin in raumfüllender Darstellung | Drahtmodell - die Elektronenwolke ist durch Punkte angedeutet |
Aminos�uren enthalten neben der Carboxylgruppe eine Aminogruppe. Bei den nat�rlich vorkommenden Aminos�uren befindet sich eine Aminogruppe am Calpha-Kohlenstoff neben der Carboxylgruppe, daneben ein Wasserstoff-Atom und einen Rest R
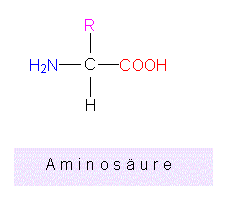
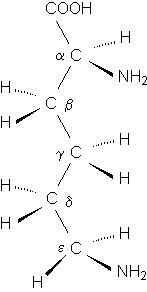
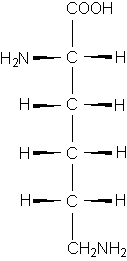
Die Formel macht deutlich, daß es sich bei den Aminos�uren um chirale Molek�le (optisch aktive Substanzen) handelt. Die überwiegende Mehrzahl der in der Natur vorkommenden und alle in Proteinen enthaltenen Aminosäuren gehören der L-Reihe an (bezogen auf Calpha, andere Kohlenstoffatome k�nnen auch chiral sein!). Am Beispiel das Lysins werden Darstellungsm�glichkeiten und Nomenklatur gezeigt:
 |
 |
 |
|
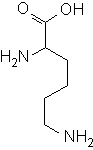
| 2,6-Diaminocaprons�ure Lysin Lys - K |
Lysin in der Fischerprojektion: L-Konformation an Calpha |
Verk�rzte chemische Schreibweise C6H10O2(NH2)2 |
Raumf�llende Ansicht C5H9CO2-(NH3+)2 |
Sowohl die Carboxyl-, als auch die Aminogruppe sind ionisierbar, so daß man es mit Zwitterionen zu tun hat:
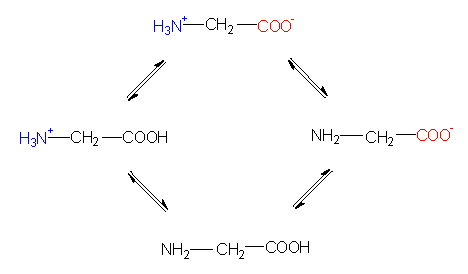
Ionisationszustände
in saurer, neutraler und alkalischer Lösung.
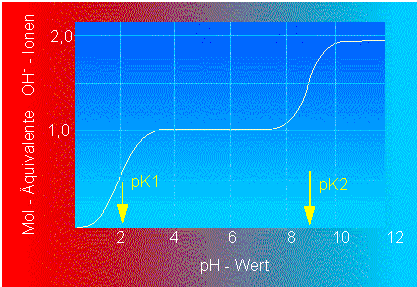
Titrationskurve des Glycins (mit zwei pK-Werten).
Die einzelnen Aminosäuren unterscheiden sich durch den Rest R voneinander. In Proteine eingebaut findet man 20 verschiedene. In freier Form, gerade auch bei Pflanzen kommen noch eine Reihe weiterer vor, von denen einige später an entsprechender Stelle vorgestellt werden.
Die 20 Aminosäuren sind durch unterschiedliche Größe, Ladung, die Fähigkeit zur Bildung von Wasserstoffbrücken und unterschiedliche chemische Reaktivität gekennzeichnet. Bei einem Teil von ihnen besteht die Seitenkette (der Rest R) aus kurzen linearen oder verzweigten nichtpolaren aliphatischen Ketten; ferner gibt es drei Aminosäuren mit aromatischen oder heterozyklischen Resten. Zwei Aminosäuren enthalten eine Hydroxylgruppe, zwei weitere das Element Schwefel. Dann gibt es wiederum je zwei mit zusätzlichen Carboxyl-, bzw. Aminogruppen und eine mit einer Imidazolgruppe. Diese Gruppen sind ionisierbar, und schließlich gibt es noch zwei, bei denen die Carboxylgruppen amidiert sind, wodurch die Ionisierbarkeit aufgehoben wird.
In der Biochemie ist es üblich, Aminosäuren durch einen Dreibuchstabencode zu bezeichnen, z.B. Gly für Glycin. Seit dem Einsatz von Computern zur Katalogisierung und Bewertung proteinchemischer Daten ist man mehr und mehr zu einer Einbuchstaben-Schreibweise übergegangen. G steht dabei für Glycin.
Hydrophobe (wasserabstoßende) nicht-polare Aminosäuren:
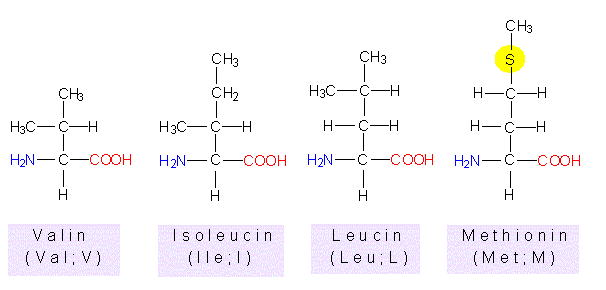
Valin, Isoleucin , Methionin
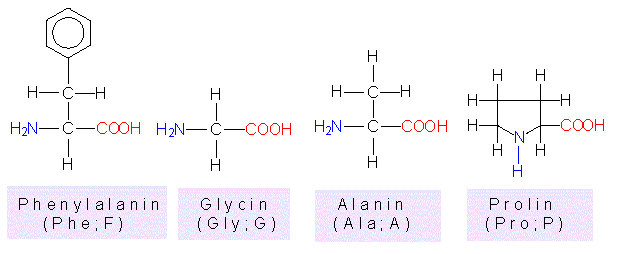
Phenylalanin, Glycin
Polare, jedoch ungeladene Aminosäuren:
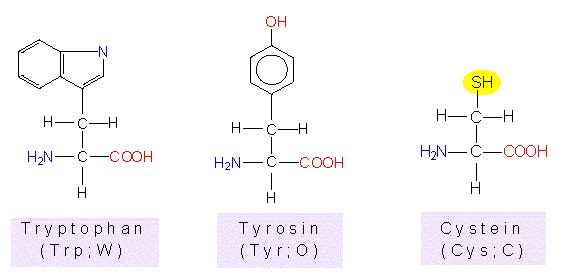
Tryptophan, Tyrosin, Cystein
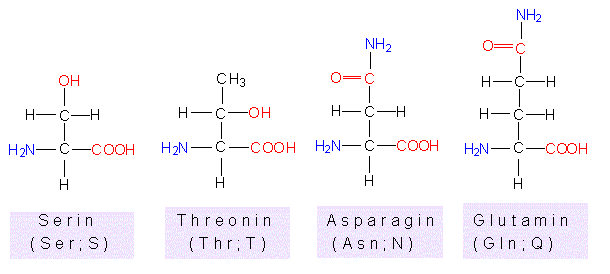
Threonin, Asparagin , Glutamin
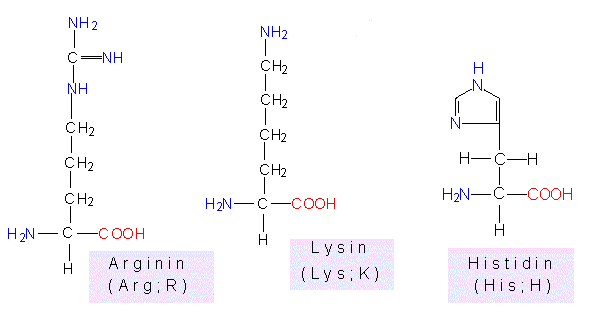
Arginin, Histidin,
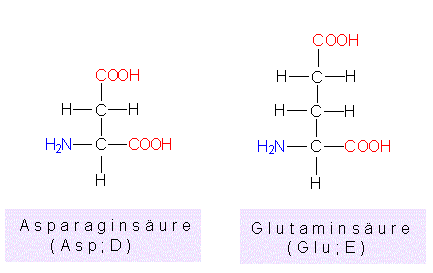
Asparaginsäure, Glutaminsäure
| Ala A | Arg R | Asn N |
Asp D | Cys C | Glu E |
Gln Q | Gly G | His H |
Ile I | Leu L | Lys K |
Met M | Phe F | Pro P |
Ser S | Thr T | Trp W |
Tyr Y | Val V | |
| acidic | ||||||||||||||||||||
| acyclic | ||||||||||||||||||||
| aliphatic | ||||||||||||||||||||
| aromatic | ||||||||||||||||||||
| basic | ||||||||||||||||||||
| buried | ||||||||||||||||||||
| charged | ||||||||||||||||||||
| cyclic | ||||||||||||||||||||
| hydrophobic | ||||||||||||||||||||
| large | ||||||||||||||||||||
| medium | ||||||||||||||||||||
| negative | ||||||||||||||||||||
| neutral | ||||||||||||||||||||
| polar | ||||||||||||||||||||
| positive | ||||||||||||||||||||
| small | ||||||||||||||||||||
| surface |
| Galerie: Aminosäuren Struktur und physikalische Daten |
|
|