Bei der bisherigen Besprechung der Photosynthese haben wir uns auf die Behandlung biochemischer Reaktionen beschränkt. Bei der Darstellung der Glykolyse und anderer Biosynthesewege wurde die Bedeutung der einzelnen Enzyme herausgestellt. So sind z.B. schon seit geraumer Zeit alle Enzyme, die für den Ablauf der Glykolyse benötigt werden, isoliert und gereinigt worden, und jeder der Teilschritte kann unter Laborbedingungen in vitro nachvollzogen werden. Natürlich bemühte man sich auch, den kompletten Satz an Komponenten zu gewinnen, die zur Photosynthese beitragen, um daraus das Gesamtsystem zu rekonstruieren. Diese Ansätze schlugen jedoch fehl, weil sie, wie wir heute wissen, von falschen Voraussetzungen ausgingen.
Eine Reihe von Problemen blieb bislang ausgespart. So wurden zwar die Begriffe "Photosystem I" und "Photosystem II" genannt, und es wurden auch die Pigmente aufgezählt, die jedes der beiden Photosysteme charakterisieren, offen blieb jedoch u.a.:
![]() Wie sieht die Organisation der Photosysteme aus?
Wie sieht die Organisation der Photosysteme aus?
![]() Wie sind die Pigmente angeordnet?
Wie sind die Pigmente angeordnet?
![]() Wieso reagiert eines der Chlorophyllmoleküle anders als
die übrigen?
Wieso reagiert eines der Chlorophyllmoleküle anders als
die übrigen?
![]() Warum stimmen Aktions- und Absorptionsspektren nicht ganz
überein?
Warum stimmen Aktions- und Absorptionsspektren nicht ganz
überein?
![]() Warum reagiert Chlorophyll a als P680 anders als P700?
Warum reagiert Chlorophyll a als P680 anders als P700?
![]() Wie sind die Elektronentransportketten mit der ATP-Bildung
gekoppelt?
Wie sind die Elektronentransportketten mit der ATP-Bildung
gekoppelt?
![]() Wie sind die Photosysteme I und II miteinander verknüpft?
Wie sind die Photosysteme I und II miteinander verknüpft?
![]() Welche strukturellen Voraussetzungen müssen realisiert
sein, damit sie miteinander kooperieren?
Welche strukturellen Voraussetzungen müssen realisiert
sein, damit sie miteinander kooperieren?
Es stand nie in Frage, daß jeder der biochemischen Reaktionsschritte durch je ein spezifisches Enzym katalysiert wird, doch dauerte es erstaunlich lange, bevor man erkannte, daß das Chlorophyll und die anderen Pigmente proteingebunden sein müssen und nur als Protein-Chlorophyll (bzw. Protein-Pigment)-Komplexe aktiv sein können. Die chromatographisch aufgetrennten - und somit isolierten - Pigmente sind für sich alleine genommen für die Photosynthese wertlos. Die Pigment-Protein-Komplexe, die (meisten) Proteine der Elektronentransportketten sowie der Katalysator der ATP-Synthese (ATP-Synthetase), sind integrale Bestandteile der Photosynthesemembran(en) (= Thylakoidmembranen bei Algen und höheren grünen Pflanzen, Cytoplasmamembranen bei photosynthetisierenden Bakterien und bei Blaualgen). Die Positionen in der Membran (z.B. innen oder außen), und die relative Anordnung der Proteine zueinander sind die wichtigsten Voraussetzungen für Energieumwandlungen.
Das gilt nicht nur für die Reaktionen der Photosynthese, sondern auch für die der Atmungskette und für die an (in) der Purpurmembran von Halobacterium halobium (einem Archaebacterium, an dessen Membran Lichtenergie - ohne einen Elektronenfluß - zur ATP-Bildung genutzt wird) lokalisierten Enzyme.
Die Ansprüche für eine Energieumwandlung sind noch höher: Benötigt werden völlig intakte, protonenundurchlässige Membranen, die ihrerseits Kompartimente umschließen, so daß ein elektrochemischer Gradient zwischen innen und außen aufrechterhalten werden kann. Einer ATP-Bildung liegt eine gerichtete Protonendislokation zugrunde, der eine pH-Änderung in einem der Kompartimente und eine Änderung des Membranpotentials parallel laufen.
Das Studium der Proteine, die für die Photosyntese essentiell sind, setzte erst sehr spät ein. Die Ursache dafür liegt darin, daß es sich durchweg um membrangebundene Proteine handelt, deren Isolierung und Charakterisierung mit den klassischen Methoden der Proteinanalyse kaum oder gar nicht gelang.
Erst nach Entwicklung empfindlicher Verfahren, wie der Gelelektrophorese und dem kontrollierten Einsatz von Detergentien (z.B. Natriumdodecylsulfat: SDS), wurde es möglich, die Proteine aufzutrennen und zumindest als Banden in einem Gel zu identifizieren. Ein Beiprodukt dieses Analyseverfahrens ist die Bestimmung der Molekulargewichte der jeweiligengen Polypeptidketten.
Ein zweiter, hiervon unabhängiger Ansatz war und ist die Verwendung spezifischer Sonden (z.B. fluorszenzmarkierter Antikörper), mit deren Hilfe es möglich ist, zu entscheiden, ob ein bestimmtes Protein (oder ein Teil einer Polypeptidkette) an der Innen- oder der Außenseite einer Membran exponiert ist. Ein Einsatz von Antikörpern gegen bestimmte Proteine erlaubt es auch, das betreffende Protein aus einem Proteingemisch selektiv auszufällen, weil nur dieses den hochspezifischen Antigen-Antikörper-Komplex ausbilden kann.
Durch vernetzende Agentien ist es möglich, Nachbarschaftsbeziehungen aufzuklären. Und durch Einsatz spezifischer Inhibitoren kann ihr Wirkungsort lokalisiert werden. So wird z.B. DCMU [3-(3',4'-Dichlorphenyl)-1,1 -Dimethylharnstoff] (Urea = Harnstoff) seit Jahren dafür verwendet, das Photosystem II zu hemmen. Da es keinen Einfluß auf das Photosystem I hat, haben ARNON und Mitarbeiter es seinerzeit als wichtiges Hilfsmittel genutzt, um die Elektronentransportkette, die vom Photosystem I ausging, getrennt von der zu studieren, die vom Photosystem II induziert wurde.
Inzwischen weiß man, daß das DCMU nicht am Chlorophyll selbst, sondern an einem Protein - dem Plastochinon bindenden Protein - angreift.
Ein dritter Ansatz zur Charakterisierung der Photosynthesemembran ist die Analyse bestimmter Mutanten. Die einzellige Alge Chlamydomonas reinhardii bot sich als Versuchsobjekt an. Man kennt eine ganze Anzahl von Mutanten mit Photosynthesedefekten, die sich vier Klassen zuordnen lassen:
- Mutanten mit einem Defekt im Photosystem I
- Mutanten mit einem Defekt im Photosystem II
- Mutanten mit einem Defekt in der Photophosphorylierung
- Mutanten mit einem Defekt in der Lichtfalle (Antenne), dem Lichtsammlerkomplex
Auffallenderweise sind nahezu alle Mutanten nicht nur durch den Verlust oder die Veränderung einer bestimmten Polypeptidkette gekennzeichnet, sondern gleich durch den Ausfall eines ganzen Komplexes (z.B. des PS I). Die Mutationen führen demnach zu pleiotropen Effekten. Mit anderen Worten: Bei Veränderung (oder dem Fehlen) einer Polypeptidkette funktioniert die Zusammenlagerung (das Assembly) der übrigen Polypeptidketten zu funktionalen Einheiten nicht mehr. Diese Beobachtung macht deutlich, wie eng die Wechselwirkung zwischen den einzelnen Polypeptidketten und wie wichtig diese für ihre Kooperation untereinander ist.
Ein weiteres, aber nicht minder wichtiges Verfahren ist die Elektronenmikroskopie, meist genutzt in Kombination mit der Gefrierätztechnik.
Die Sequenzierung von Membranproteinen bleibt nach wie vor schwierig. Doch über den Umweg der Nukleotidsequenzierung der entsprechenden Gene konnten in den letzten Jahren die Aminosäuresequenzen der meisten der an der Photosynthese beteiligten Proteine ermittelt werden. Das bemerkenswerteste Ergebnis ist der Befund, daß diese Proteine (wie übrigens auch Proteine aus tierischen oder bakteriellen Membranen) einen hohen Anteil an alpha-Helix besitzen. Die Länge der Helices entspricht der Dicke der Membran. Die einzelnen Helices sind durch Sequenzabschnitte aus polaren und/oder nichthydrophoben Aminosäuren untereinander verbunden.
Aus Photosynthesemembranen mehrerer Arten unterschiedlicher systematischer Gruppen (Angiospermen, Gymnospermen, Algen, Bakterien) sind verschiedene chlorophyllbindende Proteine isoliert und charakterisiert worden. Die bekanntesten, im Laboratorium von J. P. THORNBER an der University of California in Los Angeles bearbeiteten Proteine sind das P700-Chlorophyll-a-Protein 1 und das Lichtsammler-Chlorophyll-a/b-Protein 2. Beides sind stark hydrophobe integrale Membranproteine. Beide binden Chlorophyll a, doch nur letzteres darüber hinaus auch Chlorophyll b. Das P700-Chlorophyll-a-Protein 1 enthält das Reaktionszentrum (P700) für das Photosystem I, d.h., eines der Chlorophyllmoleküle ist in einer spezifischen Konfiguration gebunden und befindet sich in einer Umgebung (bedingt durch eine spezifische Aminosäurezusammensetzung und Faltung der Polypeptidkette), durch die es sich von allen übrigen auch an dieses Protein gebundenen Chlorophyllmolekülen unterscheidet. Diese strukturelle Besonderheit bildet die Voraussetzung für die lichtbetriebene Anregung und damit die Induktion eines Elektronenflusses.
Das Molekulargewicht der Polypeptidkette beträgt 110 000; insgesamt kann sie 14 Chlorophyllmoleküle binden. Das Lichtsammlerprotein (Lichtsammler-Chlorophyll-a/b-Protein 2) ist ebenfalls häufig und weit verbreitet. Es ist vorwiegend mit dem Photosystem II assoziiert, doch wurden auch Wirkungen auf das Photosystem I beobachtet. Chlorophyll a und b werden in äquimolaren Mengen neben Lutein und beta-Carotin gebunden. Das Chlorophyll-Carotinoid-Verhältnis beträgt auf molarer Basis 3 - 7: 1.
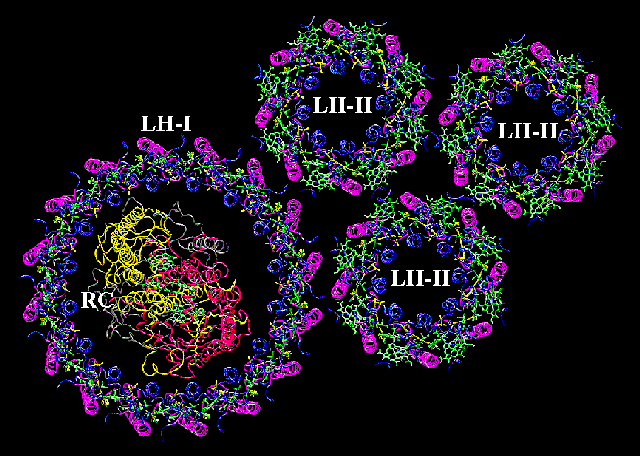
©: Theoretical Biology Group - University of Illinois at Urbana-Champaign
Zu den Aufgaben des Proteins gehört die Lichtfallenfunktion (Antennenfunktion), also die Weiterleitung von Photonen ans Reaktionszentrum (hier P680). Jenes scheint mit einem Polypeptid des Molekulargewichts 41 000 verknüpft zu sein: Chlorophyll-a-Protein 3. Chloroplasten in den Zellen der Gefäßbündelscheide des Mais (und anderer C4-Pflanzen) enthalten nur wenig oder überhaupt kein Lichtsammlerprotein.
Zur Synthese von ATP benötigt man eine ATP-Synthetase als Katalysator. Da ATP-Bildung nicht nur ein Ergebnis der Photosynthese ist, sondern auch bei der Atmungskette anfällt, lag der Gedanke nahe, daß die ATP-Bildung in beiden Fällen auf gleichartigen Mechanismen beruht.
E. RACKER von der Cornell University isolierte - nach einschlägigen Erfahrungen mit der mitochondrialen ATP-Synthetase - aus Thylakoidmembranen ein Enzym, das dem aus Mitochondrien weitgehend ähnelte. Elektronenmikroskopisch war es als ein gestielter Knopf zu charakterisieren. Der Knopf erhielt die Bezeichnung CF1 und der Stiel CF0 (F1, resp. F0 bei dem Enzym aus Mitochondrien). CF0 (bzw. F0) dient der Verankerung in der Membran. Während der F1 - F0- Komplex bei den Mitochondrien in der inneren Membran lokalisiert ist und die Köpfe in die mitochondriale Matrix hineinragen, sitzen die entsprechenden Molekülteile von CF1- CF0 an der Außenseite der Thylakoidmembranen. In beiden Fällen besteht die ATP-Synthetase aus mehreren unterschiedlichen Polypeptidketten; wir haben es also wieder mit einem Enzymkomplex zu tun. Die Phosphorylierung (von ADP) gelingt nur, wenn die ATP-Synthetase Bestandteil intakter, protonendurchlässiger Membranen ist. Wichtig ist dabei auch, daß die Membran zwei Kompartimente (Vesikelinneres und Umgebung) voneinander trennt.